心筋症:拡張型心筋症(DCM)
拡張型心筋症(DCM)
心臓が悪くなる原因はないのに、「心室が拡大して、収縮能が障害されている心臓」が拡張型心筋症(DCM、Dilated CardioMyopathyの略称)です。左心室、または左心室と右心室の両方の内腔が拡大していることが形態的な特徴です。心室の収縮能は、び慢性に(全体的に一様に)低下するのが典型的です。左心室の壁の厚さは、正常ないしは正常よりも薄いです。
画像は横にスクロールします。
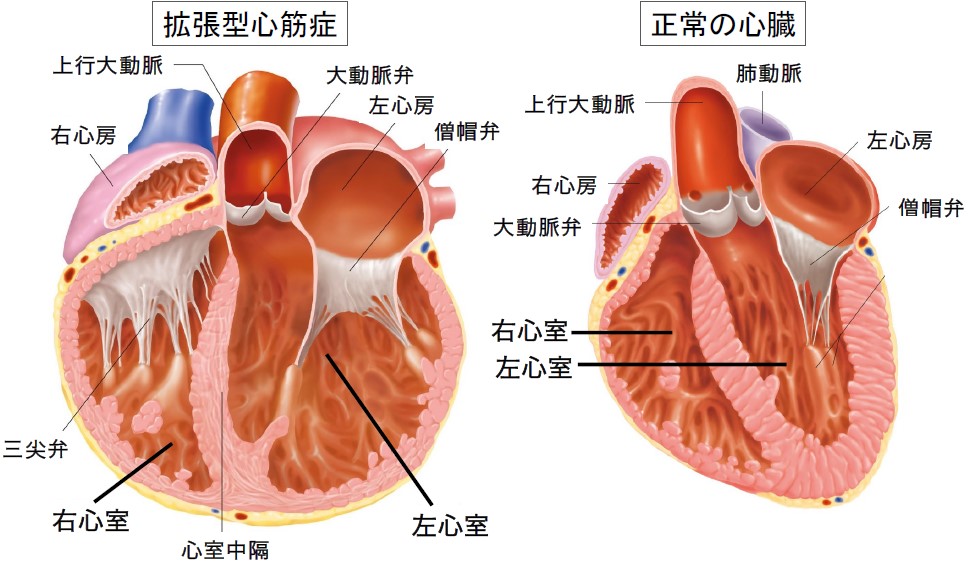
拡張型心筋症(DCM)の心臓と、正常の心臓のイメージです。DCM(左)では、左心室と右心室が拡大し、左心室の壁の厚さは正常の心臓(右)よりも薄いです。左心室の拡大に伴い、僧帽弁が下方に引っ張られて閉じにくくなると、二次性(機能性)僧帽弁閉鎖不全症を生じます。
出典:インフォームドコンセントのための心臓・血管病アトラス(一部改変)
我が国では、心不全の原因の15〜20%がDCMです。令和5年度末の時点でDCM(厚生労働省の指定難病「特発性拡張型心筋症」)の認定を受けていた患者数は18,108人でした(令和5年10月1日現在の日本の人口は、約1億2435万人)。しかし、症状がなく病院を受診していない患者さんも少なくないので、実際の患者数はもっと多いはずです。
男性に多い傾向があります(男女比は 2.6:1)。40代から60代に多いですが、子供から高齢者まで幅広い年齢層でみられます。一部のDCMには遺伝性があり、平成11年の厚生省の全国調査では約5%に家族内発症がありました。家族性DCMの約20%に、遺伝子変異(収縮蛋白や心筋細胞接合蛋白の遺伝子変異が主)があるとされています。遺伝性じゃないDCMの成因は今のところ不明ですが、ウイルス感染や免疫異常(自己免疫)の関与が示唆されています。
心不全や不整脈の症状がありますが、無症状のことも多いです
DCMに特徴的な症状はなく、主に心不全と不整脈の症状を認めます。左心室の収縮能低下が高度でも、全く無症状の場合が意外に多いです。
心不全の症状には、労作時の息切れ・倦怠感、手足や顔のむくみなどがあります。最初のうちは、階段や坂道を登った時に息が切れる程度ですが、進行すると少し歩いただけでも息苦しくなり、さらに悪化すると家庭内での日常生活にも支障をきたします。治療がうまくいって心不全がコントロールされれば、症状はなくなり落ち着いた状態に戻ります。この「落ち着いた状態」は長く続くこともありますが、心不全が徐々に進行するのに伴い「退院しても、またすぐ悪くなって再入院」という具合に入退院を繰り返すようになります(本コラムの「心不全」の「心不全は、何が悪いの?」をご参照ください)。
不整脈の症状としては、ドキドキ感(動悸)や脈が飛ぶのを感じたりします。心室を起源とする頻脈性不整脈である心室頻拍は、失神や突然死の原因になることがあります。
診断では、心エコー検査が重要です
診断のきっかけになるのは、心不全や不整脈による自覚症状や、健診などで見つかる心電図や胸部X線の異常です。心電図でよくみるのは、軽度の波形の変化(ST-T変化)です。心室性期外収縮・心室頻拍や、脈がゆっくりとなる房室ブロックなどの不整脈を認めることもあります。胸のX線写真では、多くの場合、心拡大のため心臓が大きく映ります。心不全になると、肺のうっ血(血液のうっ滞)や胸水を認めます。
診断の決め手は、心エコー検査です。左心室の内腔拡大と、収縮性の低下が確認できます。左心室壁の動きは、びまん性に一様に低下するのが典型的ですが、部位によって収縮のタイミングがずれていることもあります。右心室や心房も拡大していることが多いです。
心臓カテーテル検査では、心拍出量は低下し、血液のうっ滞(うっ血)のため左心室の拡張期の内圧(充満圧)が上昇します。虚血性心疾患(冠動脈疾患)ではないことを確認するため、冠動脈造影検査を行います。冠動脈造影検査は入院が必要ですが、外来で行える冠動脈CT検査でも冠動脈の動脈硬化の様子が確認できます。DCMの診断は、心室が拡大し収縮能が低下する二次性心筋症を一つ一つ否定する除外診断が基本です。しかし、多くの心臓病は最終的に収縮能が低下し心室が拡大するので、DCMと診断された中に二次性心筋症が紛れ込む可能性を完全には否定できません。
無症状でも、心不全の治療を行います
障害された心筋を、元の正常な心筋に戻す根本的な治療はありません。積極的な治療は、心不全と不整脈に対して行います。心不全の一般療法として、アルコールは禁止し、塩分を制限して、過度の運動は避けるようにします。しかし、心不全であっても、症状が出ない(きつくない)範囲で体を動かした方が良いです。心臓リハビリは心不全にも有益で、身体活動度を高め生命予後を改善させることが確認されています。
心不全には、主に薬物療法(内服治療)を行います。無症状のDCMにも、心不全の治療を行います。標準的な心不全治療薬は、①アンギオテンシン変換酵素阻害薬・アンギオテンシン受容体拮抗薬のいずれか、②β遮断薬(カルベジロールまたはビソプロロール)、③ミネラルコルチコイド受容体拮抗薬、さらに近年、④SGLT-2阻害薬(糖尿病治療薬ですが、心不全にも有益なことが確認されました)と、⑤サクビトリル・バルサルタンが新たに加わりました。これらの薬により、心不全の生命予後が改善することが分かっています。詳しくは、本コラムの「心不全の治療」の「左室駆出率が低下した慢性心不全(HFrEF)の治療」をご覧ください。
不整脈の治療では、心室性不整脈の対応が重要です
心房細動は、心不全の原因でもあり、心不全を悪化させる増悪因子でもあります。心不全に合併した心房細動をカテーテルアブレーションで治療すると、左心室の収縮能が改善しBNPまたはNT-proBNPが低下します。さらに、「全死亡(心不全死や不整脈死に限らない全ての死亡)」と「心不全による再入院」が減ることがわかっています。
DCMの死因の30~40%は突然死であり、その主な原因は心室細動や心室頻拍などの心室性不整脈です。これらの心室性不整脈による突然死の予防には、植込み型除細動器(ICD)が最も有効です。心室細動あるいは持続性心室頻拍のため突然死に陥る前に救命処置を受けて助かった場合は、再発の可能性が高く(年率約10%)ICDの適応です。
その他の突然死のリスク因子には、高度の収縮能低下と心不全の重症度があります。薬物治療を十分に行った後も、収縮能低下が悪いままで改善しない場合や、心不全症状がとれない場合はICD植え込みを検討します。このような場合は、ICDを植え込んだ方が、ICDを植え込まなかった場合に比べて突然死を含む全死亡が少なくなることが分かっています。
心不全が治らなくなったら、心臓移植を考える必要があります
心不全治療を最大限に行なっても病状の改善がなく、「心臓移植以外に命を助ける方法がない」という末期的な心不全には、心臓移植を考える必要があります。心臓移植の適応条件には、移植後の免疫抑制療法に対して心理的・身体的に耐えられるか、心臓移植について本人と家族の十分な理解と協力が得られるかなどが挙げられており、「年齢は65歳未満が望ましい」とされています。
1997年10月に臓器移植法が施行され、1999年2月に第1例目の心臓移植が行われました。しかし、2009年までの移植件数は年間10前後でした。2010年7月に臓器移植法が改正され、本人の意思が不明の場合でも遺族の同意があれば臓器提供が可能となり、15歳未満の方からの臓器提供も可能となりました。心臓移植の累計件数は、第一例目から2010年の法改正までの11年間は69例でしたが、法改正から13年後の2023年12月には819例となりました。 2022年12月までの累計704件の心臓移植の集計では、18歳以上の患者さんは636人で、最も多い原因疾患はDCMでした(62%)。移植後5年・10年・15年の生存率は、それぞれ93%・89%・80%でした。一方、国際心肺移植学会の登録データ(1992年1月〜2017年6月の114,783件の心臓移植)では、移植後5年・10年・15年の生存率は72%・57%・39%でした。我が国の心臓移植の成績は、国際的にもかなり良好です。
人工心臓が、心臓移植に代わる治療法として注目されています
左室補助人工心臓(LVAD)は、弱った心臓の代わりに、左心室から吸引した血液を大動脈に送血して左心室の働きを補助する医療機器です。体外のポンプに血液を引き込み体内に戻す「体外式」と、体内にポンプを植え込む「植込み型」があります。かつて、LVADの使用が認められていたのは、心臓移植手術までの待機期間だけでした。
体外式は、大型の器械に繋がれるため退院は不可能で、病院内で待機できる患者数には限界がありました。その後、植込み型LVADが実用化されました。植込み型は耐久性が高い上に合併症が少なく、退院して自宅で心臓移植を待つことができます。そのため、心臓移植を待つ待機患者さんが増えました。
しかし、それに見合う心臓移植件数の増加がなかったので、待機期間は平均1877日(2022年現在)とかなり長期化しました。待機期間が長くなったのは残念なことでしたが、植込み型LVADの長期の有用性と安全性が実証された形となりました。
最重症の心不全は、適切に治療されなければ、2年以内に50%の患者さんが亡くなるといわれています。LVAD治療は、このような患者さんの生命予後を改善します。我が国で、LVADを植え込んで心臓移植を待つ患者さんの生存率は、1年後は約90%、3年後は約80%でした。
2021年に、心臓移植を前提としないLVADの使用が医療保険で認められました。対象となるのは、心臓移植が妥当と判断されながら、「65歳未満が望ましい」という年齢制限のために心臓移植の対象から外れていた患者さん。さらに、高度の肝障害や腎障害のために心臓移植の対象とならなかった患者さんです。心臓移植に代わるLVAD治療を、Destination Therapy(DT、長期在宅補助人工心臓治療)といいます。心臓移植や、植込み型LVADによるDTを行うことができる病院は限られています。我が国で心臓移植を行っているのは大学病院を中心とした12施設(2025年8月現在)、DTを行っているのは22施設(2025年5月現在)です。2025年10月現在、心臓移植希望登録者数(いわゆる待機患者数)は795人です。待機患者さんのLVAD装着率は、心臓移植を受ける時点ではほぼ10割ですが、待機患者さん全体では6〜7割と推測されます。
参考資料
- 日本循環器学会/ 日本心不全学会合同ガイドライン 心筋症診療ガイドライン(2018年改定版)
- 日本循環器学会/ 日本心不全学会合同ガイドライン 急性・慢性心不全診療ガイドライン(2017年改定版)
- 日本循環器学会/ 日本心臓血管外科学会/日本胸部外科学会/日本血管外科学会合同ガイドライン 重症心不全に対する植込型補助人工心臓治療ガイドライン(2021年改訂版)
- 日本循環器学会/ 日本心不全学会/ 日本小児循環器学会合同ガイドライン 心臓移植に関するガイドライン(2025年改定版)
[心筋症 関連記事]



